Урок физики в 10 классе «Первый закон термодинамики»
Автор: Людмила Васильевна Палилкина
Организация: МБОУ «Мокшинская СОШ»
Населенный пункт: Омская область, Любинский район, Веселая Поляна
Урок физики в 10 классе «Первое начало(закон) термодинамики» - урок изучения нового материала
1.Формулирование темы
Шел за окном 1840 год. Из Германии отправлялось судно к острову Ява. А судовым врачом на этом судне был Роберт Майер. Во время лечения матросов кровопусканием он обратил внимание на то, что венозная кровь у них была светлее, чем обычно бывает у людей в северных широтах, и приближалась по яркости к артериальной. Ничего не хотите у меня спросить? Не перепутала ли физику с биологией, например? Он заметил: «Кровь, выпускаемая из ручной вены, отличалась такой необыкновенной краснотой, что, судя по цвету, я мог бы думать, что попал на артерию». Тогда Майер предположил, что «температурная разница между собственным теплом организма и теплом окружающей среды должна находиться в количественном соотношении с разницей в цвете обоих видов крови, то есть артериальной и венозной… Эта разница в цвете является выражением размера потребления кислорода или силы процесса сгорания, происходящего в организме». Говоря простым языком, по разнице в цвете крови можно понять, сколько кислорода потребил (т.е. сжёг) организм. (Чем отличается венозная кровь от артериальной и почему?)
Прибыв в родной Хайльбронн, Майер в 1842 году опубликовал в журнале «Анналы химии и фармациѝ» свою работу «Замечания о силах неживой природы». В ней он указал на эквивалентность затрачиваемой работы и производимого тепла и тем самым обосновал первый закон термодинамики.
Это и будет темой нашего урока: «Первое начало(закон) термодинамики» - Запишите
2.Формулирование цели
Т.е., если изучаем ЗАКОНЮ то что будет целью? – Изучить первый закон термодинамики.
3.Формулирование задач
А что нужно сделать, чтобы изучить закон(вы уже это знаете), вспоминайте?
А). Между какими явлениями (процессами) или величинами закон выражает связь. Единицы измерения величин.
Б). Словесную формулировку закона.
В). Математическое выражение закона.
Г). Опыты, подтверждающие справедливость закона.
Д). Примеры применения закона на практике. – Это наши задачи.
4.Формулирование планируемых результатов
Теперь переформулируем наши задачи, чтобы они стали нашими планируемыми результатами. Т.е что мы должны уметь делать:
А).Перечислять величины, входящие в закон.
Б).Формулировать первый закон термодинамики.
В).Записывать формулу, выражающую первый закон термодинамики.
Г).Объяснять опыты, подтверждающие первый закон термодинамики.
Д).Приводить примеры применения первого закона термодинамики на практике. – Запишите.
5. Актуализация знаний – «Холодный обзвон»:
- Напишите на доске формулу ИЗМЕНЕНИЯ ВНУТРЕННЕЙ ЭНЕРГИИ.
- Напишите формулу РАБОТЫ В ТЕРМОДИНАМИКЕ.
- Напишите связь между РАБОТОЙ ТЕРМОДИНАМИЧЕСКОЙ СИСТЕМЫ И РАБОТОЙ ВНЕШНИХ СИЛ.
6.Изучение нового материала
А).Познакомимся с Первым законом термодинамики(видео – 2 мин) https://www.youtube.com/watch?v=MhQYrG09p1g)
Б). Систематизация материала – составление таблицы самостоятельно индивидуально(4 обучающихся находят в параграфе материал каждый про свой процесс(изотермический, изобарный, изохорный, адиабатный): каковы его особенности, и как применительно для этого процесса будет выглядеть I закон термодинамики.
Проверка:
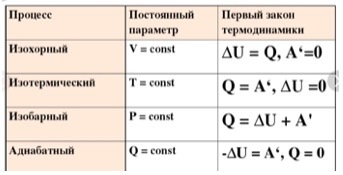
В).Объяснение опытов, подтверждающих I закон термодинамики
- Огниво – 1,5 мин. https://www.youtube.com/watch?v=PXB_dRfZG70
- Туман в бутылке – 1,5 мин. https://www.youtube.com/watch?v=GvuQWk84HTw
7.Закрепление. Решение задач: (№1 а) и б) с места объясняем, №2 – решаем у доски)
№1.Определите процессы, в которых участвует термодинамическая система идеальный газ, и прочитайте уравнение первого закона термодинамики для каждого случая?
а) 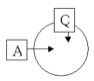
Ответ: происходит теплопередача, и над газом совершается работа, то есть изменяется объём, давление, температура, внутренняя энергия газа: U=Q+A.
б) 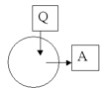
Ответ: газу сообщается количество теплоты, следовательно газ совершает работу, то есть объём газа увеличивается; в зависимости от значений Q и А происходит изменение внутренней энергии: U=Q-A.
№2.При адиабатическом сжатии газа была совершена работа 200 Дж. Что произошло при этом с внутренней энергией газа? ( ΔU = – 200 Дж)
Самостоятельная работа:
|
1 вариант (Проверяем друг у друга, затем отчет перед классом)
2.При изохорном нагревании газу было передано от нагревателя 250 Дж теплоты. Какова работа, совершенная газом? Что произошло с его внутренней энергией? (Aʹ= 0; ΔU = 250 Дж)
|
2 вариант (Проверяем друг у друга, затем отчет перед классом) 1. Определите процесс, в котором участвует термодинамическая система идеальный газ, и прочитайте уравнение первого закона термодинамики для этого случая?
2.Идеальный газ, находясь в тепловом контакте с окружающими телами, совершил работу 300 Дж. При этом внутренняя энергия газа увеличилась на 300 Дж. Получал или отдавал газ количество теплоты и сколько? |
1 вариант: Ответ: газ нагревается, внутренняя энергия увеличивается, давление увеличивается, объём остаётся прежним: U=Q.
2 вариант:Ответ: газ охлаждается, и над ним совершается работа, то есть возможно изменение внутренней энергии: U=А - Q.
8.Подведение итогов, рефлексия:
Чего должны достичь? Посмотрите планируемые результаты. Пройдем по всем пунктам… Справились? Что осталось непонятным? Какие вопросы?
9.Выставление оценок:
Анализ систематизации материала учебника и результатов самостоятельной работы.
10.Домашнее задание: § 80-81, упр. 15 (2-3).